CTMS 使组织能追踪和管理其临床试验运营。CTMS 属于 Vault Clinical Operations 系列应用程序。在单个 Vault 中,您的组织可以拥有一个、两个或所有这些应用程序。这些应用程序共享一个通用数据模型,但每个应用程序都提供额外的功能来帮助管理临床试验流程。
CTMS Vault 提供以下功能:
- 研究经理主页:为研究经理提供可查看研究、研究国家/地区和研究站点级别的关键信息、状态、指标和数据的页面。
- 研究管理:提供跟踪和管理整个研究中的事件、里程碑、指标、绩效和合规性的能力。
- 问题管理:提供采集、跟踪和管理观察结果、风险缓解措施、方案偏差和跟进研究项目的能力。
- CRA 主页:为 CRA 提供可查看包括研究、研究国家/地区和研究站点级别的关键信息(包括状态、注册指标、偏差和监查访视)的页面。
- 站点监查:提供管理常规监查访视(研究前访视、站点启动访视、中期监查访视和结束访视)的所有方面的能力,包括确认和跟进信函、监查访视报告以及跟踪站点监查活动。
- 研究通信:提供管理研究人员及其联系信息,并追踪与研究有关的所有通信的能力。
- CDMS 和 Clinical Operations Vault 的连接:允许从 Clinical Operations CTMS Vault 到 CDMS EDC Vault 交换研究、研究国家/地区和站点,以及从 EDC Vault 到 CTMS Vault 交换受试者、受试者访视、程序和访视定义。
- 受试者访视:为研究经理提供定义研究访视、创建和跟踪给定受试者的访视和相关源数据验证 (SDV) 活动,并在监查报告和其他研究管理报告中使用这些数据的能力。
- Vault Payments:使研究经理能够管理与试验相关的付款请求、费用和预算。
- 临床试验通知:提供生成 Yuzu 临床试验通知 (CTN) 并将其提交给日本卫生局 (PDMA) 的能力。
- 基于风险的研究管理 (RBSM):为研究团队提供创建、审查和批准研究特定风险评估的能力。
数据模型
CTMS 共享具有 eTMF 和 Study Startup Vault 的通用数据模型组件,这使组织能够将所有 Clinical Operations 应用程序的数据整合到 Vault 中。此外,还有一组 CTMS 特定对象和一组支持对象。支持对象包含的数据大多是静态或自动填充的。用户通常不会为支持对象创建记录。
CTMS 对象
除共享 数据模型外,CTMS 应用程序还拥有用于存放数据的其他对象。以下是一份核心 CTMS 对象列表,但并非所有对象都包含在内。
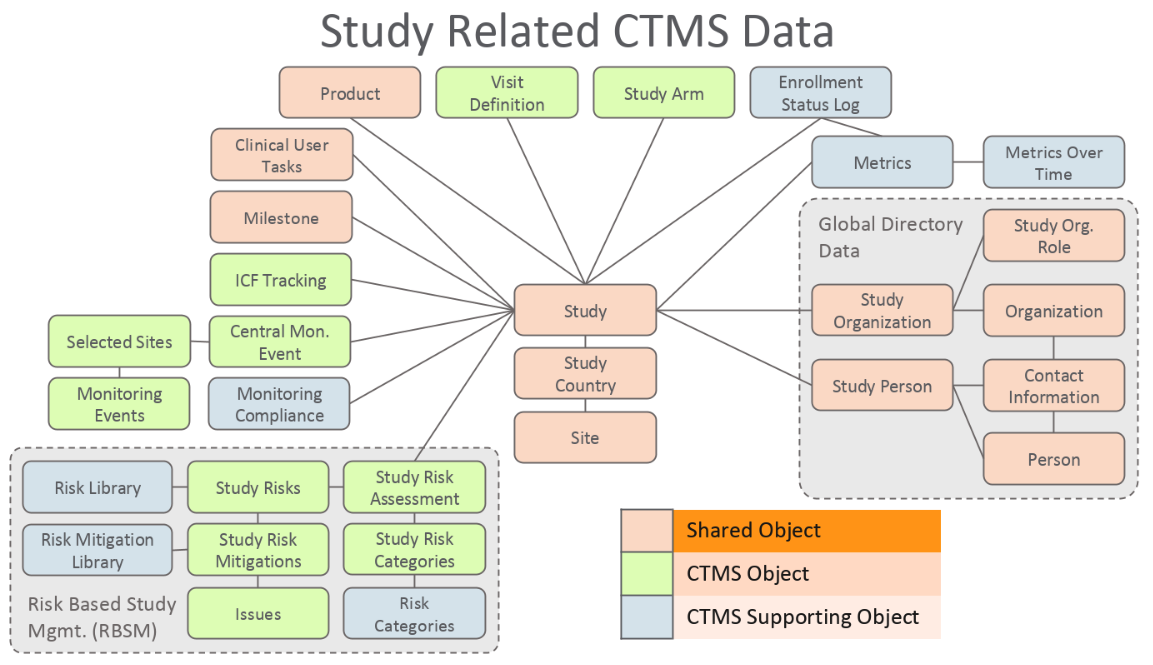
研究相关对象
- 访视定义:该对象定义了受试者在本次试验过程中在 CTMS 内可以参与的访视类型。访视定义用于临床试验过程中的受试者访视,包括筛选访视、每月访视、试验结束访视等。
- 试验组:该对象追踪可用于研究的研究组。管理员可将受试者关联至为研究定义的试验组。
- ICF(知情同意书)追踪:知情同意跟踪对象追踪给定试验的主“知情同意书”,包括其版本和版本日期。Vault 将此对象与知情同意站点有效追踪对象结合使用,以跟踪临床站点的 IRB 或 EC 对“主知情同意书”的批准。
- 中央监查事件:该对象追踪监督监查事件,其中研究团队希望跟踪多个研究站点的问题和结果。
- 活动:该对象追踪与人员的交互。活动可以在临床研究的范围内或范围外进行记录。
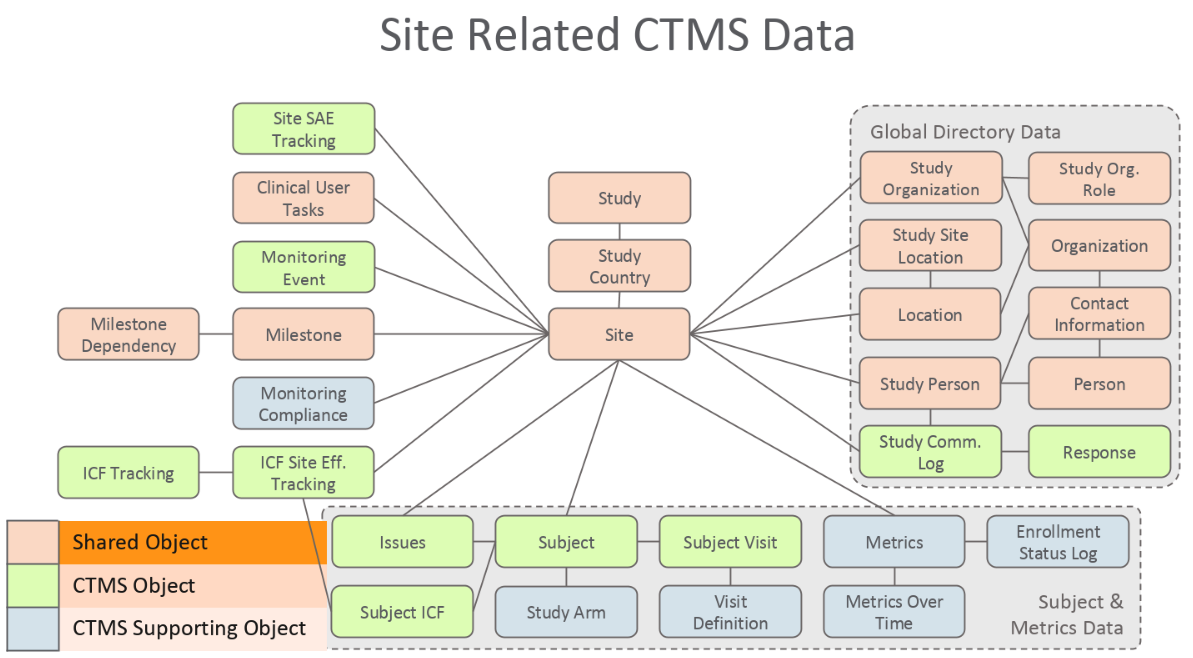
站点相关对象
- 指标:该对象包含研究、研究国家/地区和站点的计划、预测和实际注册人数及绩效指标。在添加受试者、受试者状态更改或研究、研究国家/地区或研究站点记录发生更改后,Vault 会自动创建或更新该对象中的记录。
- 受试者:该对象包含研究中所有受试者的列表、其当前的注册状态和适用的状态日期。该对象通常通过数据采集或随机化系统的整合或常规文件加载来填充。
- 站点 SAE 跟踪:该对象采集与此特定站点的受试者相关的“严重不良事件”信息。
- 问题 (
pdv__ctms):该对象采集与受试者、研究站点以及整个研究相关的问题信息。 - ICF(知情同意书)站点有效追踪:知情同意站点有效追踪对象追踪站点的 IRB 或 EC 对试验“主知情同意书”的批准。
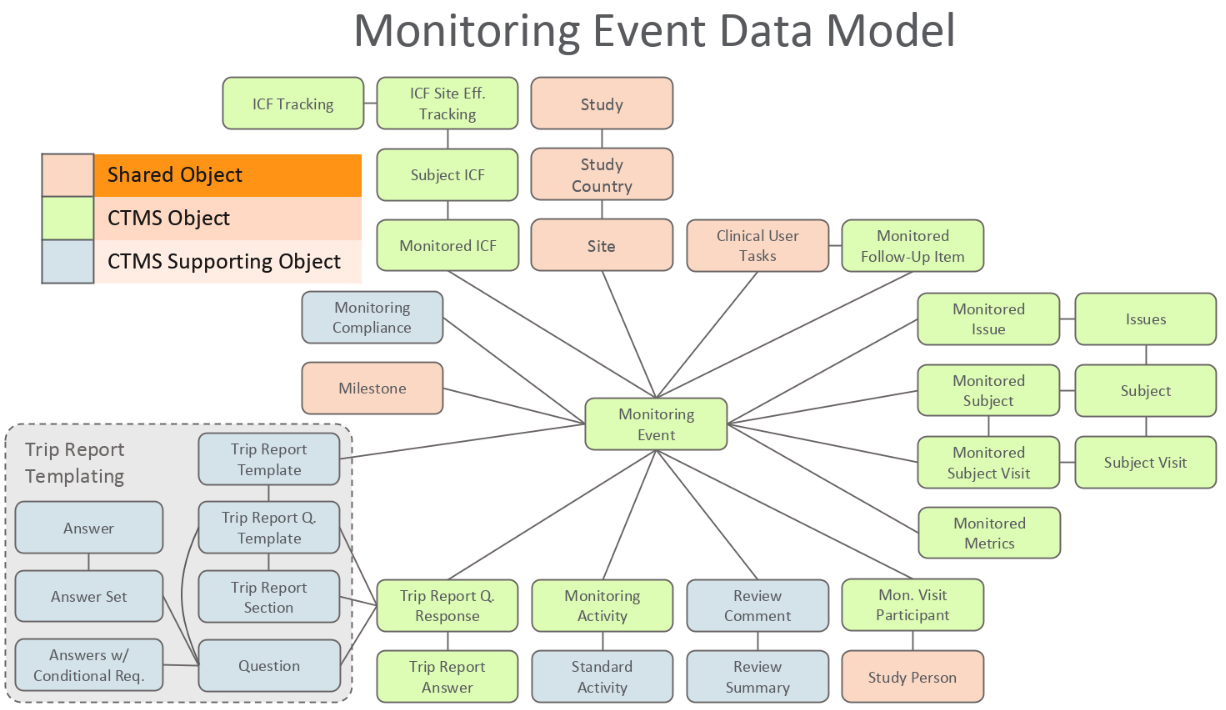
监查与事件相关的对象
- 监查事件:该对象表示监查事件。这些可能是现场访视、电话联系或远程监控活动。研究人员可以将其与相关对象(监查访视参与者、监查活动、监控的受试者、监控的知情同意书、监查事件跟进项目、监控的受试者访视)一起使用,以管理所有监查事件的计划、实施和跟进。监查事件对象也是使用行程报告的中心位置。
- 监控的受试者:该对象包含站点上受试者的快照及其在监查事件发生时的状态。如果监查员在监查访视期间发现受试者状态不正确,监查员可以添加或编辑监查事件的受试者。
- 监控的受试者访视:该对象包含站点受试者访视的快照及其相关数据,这些已经过源数据验证或需要进行源数据验证。
- 监控的 ICF(知情同意书):监控的知情同意书对象包含受试者签署“站点有效知情同意”的时间以及所签署的“主知情同意书”版本的信息。
- 监查跟进项目:监查已结束跟进项目和监查已结束跟进项目对象包含自上次监查事件以来当前未决或已结束跟进项目。
- 监查问题:该对象包含与监查事件相关的问题。
- 监查指标:该对象包含监查事件发生时该站点在试验中实际注册的快照。
- 监查活动:该对象包含在监查事件的整个过程中预期完成的活动列表。
- 监查访视参与者:该对象包含预期参与试验的站点参与者列表,以及关于他们是否受邀或参加监查事件的信息。
- 行程报告问题回复:该对象包含应向站点或执行监查事件时提出的问题和答案。
CTMS 数据模型还包括其他对象。这些对象均可供您在 Vault 中使用和配置。为了在现实世界中准确地维持这些数据元素之间的关系,数据模型包括几种多对多和父子关系,用于将对象链接在一起。
关键共享对象
该列表对数据模型中的核心对象进行了一些解释,但并不是 Clinical Operations(eTMF、Study Startup 和 CTMS)Vault 共享对象的完整列表。
- 研究人员:该对象将人员及其相应的联系信息分配给研究或研究站点和角色,使组织能够在单个列表中管理 Vault 用户和非 Vault 用户。
- 研究组织:该对象允许用户将特定角色分配到研究、研究国家/地区或研究站点层级的组织中。
- 研究通信:该对象包含所有入站和出站站点通信以及与研究相关的其他通信。相关回复对象追踪关于同一询问的相关跟进通信,研究通信跟进项目对象可以追踪、管理和上报通信中所需的操作。
- 里程碑:该对象定义、追踪和管理所有相关的研究、研究国家/地区和研究站点里程碑。里程碑还可管理预期、计划和实际监查访视开始和结束日期。
- 临床用户任务:该对象附加到临床应用程序独有的多个功能,例如任务模板和 CTMS 主页。
标准作业
CTMS 包括减少手动重新输入数据的计划作业,并计算为研究经理和 CRA 主页供电所需的指标。
- 注册状态:该作业每晚运行,并在研究经理和 CRA 主页上形成生成注册状态图所需的指标和里程碑数据快照。
- 监查合规总结:该作业每晚运行,并计算预期和过期的监查事件的数量,以及在预期时间范围内完成的监查访视报告的百分比。
自动创建对象记录
CTMS 包括以一定间隔创建对象记录的自动化过程。
- 更新指标:该作业计算实际注册率、筛选失败率、退出率以及每种状态下的受试者总数。该作业会计算站点、总体研究国家/地区和总体研究层级的这些指标。更新指标作业在站点级别触发,并在受试者状态更改后一 (1) 小时运行。这些作业包括在一小时内做出的任何更改。Vault 在国家/地区内的站点级别更改后执行此作业的研究国家/地区版本,研究国家/地区更改后执行研究版本。
- 种子监测注册:当监查事件记录设置为进行中时,该作业将运行。此数据作业使用当前受试者及其站点状态的副本,以及适用于监控的受试者中创建的受试者的当前受试者访视副本,发布监控的受试者记录。这减少了 CRA 的数据输入。
- 更新监查指标:该作业提供与更新指标作业相同的功能,但应用于特定监查事件中的受试者数据。
相关文章
阅读以下文章,了解如何使用 CTMS 应用程序:
- CRA 主页
- 研究经理主页
- 行程报告操作
- 问题管理
- 定义受试者访视
- 受试者和注册指标
- 受试者招募计划
- 基于风险的研究管理
- Clinical Operations 至 CDMS Vault 的连接
- Vault Payments
- 使用 Vault Payments 进行研究预算跟踪
- Yuzu 临床试验通知
管理员文章
阅读以下文章,了解如何配置 CTMS 应用程序: